近日,浙江省食藥監(jiān)局發(fā)布《浙江省擬不開展仿制藥質(zhì)量和療效一致性評價的品種信息》,其中共32家藥企的160個藥品計劃擬不再開展仿制藥一致性評價。
對于大多數(shù)藥企而言,一致性評價工作時間緊、評價費用昂貴,因此對手中所有品種均開展一致性評價很難實現(xiàn),而這160個品種被這些企業(yè)放棄,則意味著這項工作開展一年多來,各企業(yè)對自身工作面臨的形勢和推進程度有了更加清晰的認識,也做出了更加現(xiàn)實的決定。
國泰君安證券分析指出,按照2018年底大限,中小企業(yè)度選擇放棄相關(guān)品種,節(jié)省時間和資金用于進展較快、最有希望爭奪市場品種上,不失為明智之舉。
與此同時,這160個被制藥企業(yè)擬放棄開展一致性評價的品種一定是經(jīng)過企業(yè)管理層權(quán)衡、評估、綜合考慮后的結(jié)果。這是目前全國第一個省份統(tǒng)一公布擬放棄名單,其他省份或會跟進,這種方式方便企業(yè)更為理性篩選品種,也有利于企業(yè)理性做出選擇, 并在整體上加快仿制藥一致性評價的進展。
1、藥企:有的放棄大半品種
整體來看,涉及擬放棄品種目錄的企業(yè)數(shù)量有32家之多,其中普洛藥業(yè)旗下的浙江巨泰制藥有限公司是申報擬放棄品種數(shù)最多的公司,共計35個品種。而申報擬放棄品種數(shù)大于等于5的制藥企業(yè)共有12家,按照上市公司子公司歸并后,康恩貝、三生制藥、新光藥業(yè)、海正藥業(yè)、華海藥業(yè)等上市公司均有較多品種宣布擬放棄一致性評價。

甚至有的企業(yè)擬放棄的品種數(shù)量已經(jīng)占全書品種數(shù)量的一大半。以普洛藥業(yè)為例,其旗下子公司浙江巨泰制藥有限公司截至2017年7月底共獲得41個品種的“國藥準字”批文,而此次直接擬放棄其中35個品種的一致評價工作,只保留了頭孢克肟分散片、阿莫西林克拉維酸鉀膠囊(2個規(guī)格)、滅菌結(jié)晶磺胺、維生素E煙酸酯等品種。據(jù)悉,頭孢克肟分散片、阿莫西林克拉維酸鉀膠囊是普洛藥業(yè)的主要產(chǎn)品,其市場份額在2017年上半年保持穩(wěn)健提升,目前已備案參比制劑,BE試驗即將啟動。
再以新光藥業(yè)為例,此次擬放棄7種化學(xué)藥的一致性評價工作。據(jù)了解,該公司主打中成藥業(yè)務(wù),公司主導(dǎo)產(chǎn)品黃芪生脈飲、伸筋丹膠囊和西洋參口服液2016年合計營收占總營收比高達98.5%。因此,行業(yè)預(yù)計擬放棄7種化學(xué)藥的一致性評價對公司未來業(yè)績影響整體較小。
國泰君安證券分析指出,從目前一致性評價的進展來看,BE試驗走在前列的主要為石藥集團、上海醫(yī)藥、聯(lián)邦制藥等具備充裕資金和雄厚研發(fā)實力的大型醫(yī)藥企業(yè),中小型制藥企業(yè)度自身無力與之競爭相關(guān)品種,選擇直接放棄,節(jié)省資金用于自身進展較快、最有希望搶占市場的品種的一致性評價工作,較為明智。
2、品種:舍“小”保“大”
從被放棄的品種來看,整體浙江省公布的擬被放棄的品種的共同點在于:競爭激烈且品種是這些企業(yè)的非核心品種。據(jù)國泰君安證券研究報告分析,這160個擬放棄品種現(xiàn)有批文數(shù)目眾多,競爭激烈,絕大部分在中檢所已有較多企業(yè)進行過參比制劑備案。
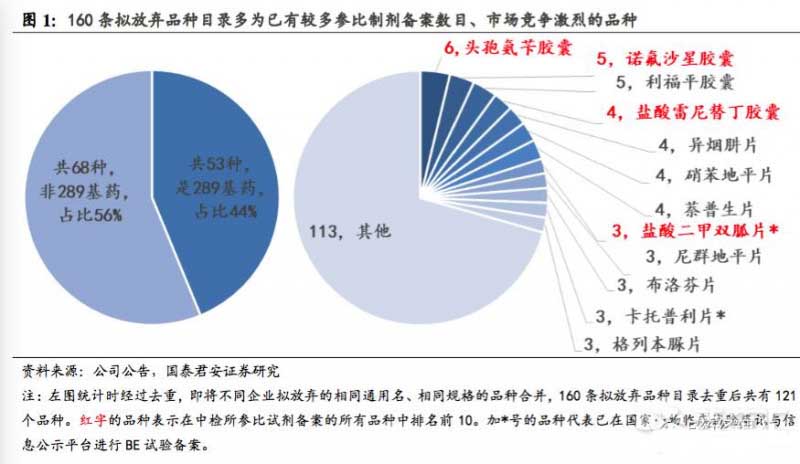
如頭孢氨芐膠囊(以通用名計)就有5家企業(yè)宣布擬放棄一致性評價。頭孢氨芐膠囊是首批“289”目錄中的基藥之一,同時也是中檢院公布的參比制劑備案數(shù)目總排名第2的品種。同時,諾氟沙星膠囊、鹽酸雷尼替丁膠囊、鹽酸二甲雙胍片等被多家企業(yè)放棄的品種也位居中檢院公布的參比制劑備案數(shù)總排名前10名。據(jù)悉,以上四個品種已有批文數(shù)目均超過100,且生產(chǎn)企業(yè)數(shù)量多,競爭激烈。
此外,還有阿莫西林膠囊、鹽酸二甲雙胍片等品種已有石藥集團、復(fù)星醫(yī)藥等大型醫(yī)藥企業(yè)完成全部BE試驗。
數(shù)據(jù)顯示,截止至2017年7月24日,中檢所共公開629家仿制藥企業(yè)備案的約4000個參比制劑備案條目,其中涉及到289個基藥目錄的有2294個,占比57%;289個基藥品種中的223個已有企業(yè)備案參比制劑,占比77%。截止2017年8月4日,160條擬放棄品種目錄(去重后是121個品種)中目前已進行BE試驗備案的約有5種,分別是:阿莫西林膠囊、 阿奇霉素膠囊、鹽酸二甲雙胍片、鹽酸克林霉素膠囊、卡托普利片, 除卡托普利片外,其余4種品種均有BE試驗已經(jīng)完成。

根據(jù)2016年3月國務(wù)院辦公廳印發(fā)的《關(guān)于開展仿制藥質(zhì)量和療效一致性評價的意見》要求:“國家基藥品種中,在2007年10月1日前批準上市的化學(xué)藥品仿制藥口服固體制劑,應(yīng)在2018年底前完成一致性評價,逾期未完成的,不予再注冊”。以及,“同品種藥品通過一致性評價的生產(chǎn)企業(yè)達到3家以上的,在藥品集中采購等方面不再選用未通過一致性評價的品種”。
因此,這些企業(yè)放棄這些品種的評價工作,也就意味著其文號將被注銷,企業(yè)將不能再銷售該品種,失去該品種目前的市場份額。但是這批擬被放棄品種均為各家上市公司的非核心品種,且這些品種的銷售占企業(yè)收入比例較低,分析認為長期來看企業(yè)選擇放棄對未來銷售收入影響整體較小。
3、未來:“剩”者為王
一致性評價進行至今,無論是監(jiān)管部門還是企業(yè)自身都對這項改革任務(wù)的重要性有了清晰和深刻的認識,也越來越秉持開放時效的態(tài)度,未來一年將是一致性評價的關(guān)鍵期,預(yù)計陸續(xù)將有品種通過一致性評價,中國制藥工業(yè)的洗牌正式開始。
6月28日,浙江省食藥監(jiān)局發(fā)布公告稱,已經(jīng)完成了對浙江京新藥業(yè)股份有限公司的瑞舒伐他汀鈣片仿制藥一致性評價的初審工作并上報國家總局。緊接著,江蘇省泰州市食藥監(jiān)局發(fā)布的文章《省食藥監(jiān)局大力推進仿制藥質(zhì)量和療效一致性評價工作》稱,截至6月中旬,江蘇省已有揚子江藥業(yè)集團等4家企業(yè)6個品規(guī)完成一致性評價,并向省局申報。如今,浙江省再次公布相關(guān)進展,可謂是走在了改革的最前方。
國泰君安證券指出,隨著一致性評價的推進,中國化學(xué)制藥產(chǎn)業(yè)去產(chǎn)能化、“剩”者為王、優(yōu)化市場競爭格局的供給側(cè)改革的春天將到來,制藥行業(yè)進入長周期新起點。尤其是工業(yè)基礎(chǔ)扎實、有一定的利潤體量、品種數(shù)量較多、重視一致性評價,且評價進展順利的優(yōu)秀治療型品種制藥企業(yè)最終會受益于行業(yè)變局的結(jié)構(gòu)性機會。
雖然短期來看,不進行一致性評價的品種將逐漸退出市場,企業(yè)將面臨銷售品種減小所帶來的利潤下行風險。然而,如能利用擬放棄各自的非優(yōu)勢品種的一致性評價工作節(jié)省下來的物力和財力快速推進自身核心優(yōu)勢品種的一致性評價工作,爭取盡早通過,則有望搶占新的市場份額,實現(xiàn)彎道超車。
一致性評價工作持續(xù)推進,品種壓縮早已經(jīng)是行業(yè)趨勢,淘汰掉小品種后剩下的將是各制藥企業(yè)最具代表性的大品種,擁有優(yōu)秀品種的制藥企業(yè)最終會受益于行業(yè)變局。雖然仿制藥一致性評價的威力可能暫時還未真正發(fā)揮出來,但是隨著越來越多的品種完成評價,留給很多企業(yè)的時間真的不多了!
(本文編輯整理自國泰君安證券研報《有的放矢,一致性評價推進加速——一致性評價浙江新動向:160 個品種擬被擬放棄》,160個品種具體信息詳見報告。)











 相關(guān)新聞
相關(guān)新聞