PROTAC技術(shù)作用機(jī)制
PROTAC技術(shù)作用機(jī)制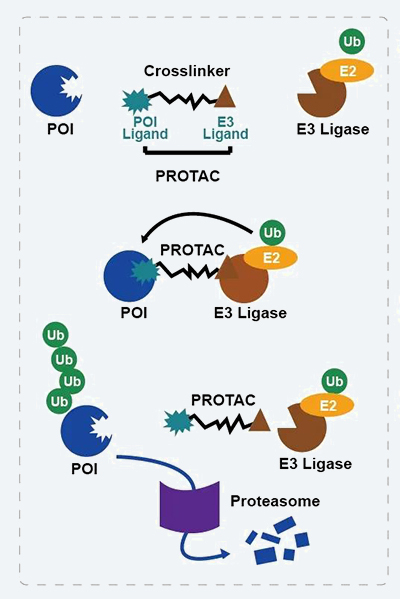
1.PROTAC分子通過(guò)其一端的靶蛋白配體(POI Ligand)特異性識(shí)別并結(jié)合靶蛋白,通過(guò)其另一端的E3泛素連接酶配體(E3 Ligase Ligand)特異性識(shí)別并結(jié)合E3 Ligase;
2.形成P O I - P R O T A C - E3 ligase三元復(fù)合體;
3. 在此三元復(fù)合體中,靶蛋白POI被E3 ligase泛素化修飾,泛素化修飾了的POI隨后被蛋白酶體識(shí)別并降解,由此抑制靶蛋白的功能。
 PROTAC技術(shù)優(yōu)勢(shì)
PROTAC技術(shù)優(yōu)勢(shì)- 改變靶點(diǎn)的“不可成藥性”(undruggable)PROTAC的作用分子機(jī)制是通過(guò)泛素-蛋白酶體系統(tǒng)降解靶蛋白,并非通過(guò)競(jìng)爭(zhēng)結(jié)合以封閉靶蛋白功能區(qū)而發(fā)揮蛋白功能抑制作用,因此PROTAC對(duì)靶蛋白識(shí)別結(jié)合區(qū)不一定非得是活性區(qū),結(jié)合力也不一定必須是高親和力;這使得一些缺乏高親和力小分子結(jié)合的“不可成藥性”靶蛋白變成“可成藥性”。
- 高效性傳統(tǒng)小分子抑制劑通過(guò)競(jìng)爭(zhēng)結(jié)合靶蛋白活性功能域而抑制靶蛋白功能,所需小分子的量往往較大;而PROTAC通過(guò)泛素-蛋白酶體系統(tǒng)降解靶蛋白以解除靶蛋白功能,故具有可循環(huán)使用性、用量低和高效性的特點(diǎn)。
- 無(wú)免疫原性與抗體藥物相比,PROTAC不會(huì)引發(fā)抗藥抗體產(chǎn)生。
 美迪西PROTAC技術(shù)服務(wù)
美迪西PROTAC技術(shù)服務(wù)- PROTAC設(shè)計(jì)合成美迪西有著多年的PROTAC合成經(jīng)驗(yàn),匯總了當(dāng)前熱門的多種POI配體,不同組織類型的E3 Ligase配體,并且建立了含數(shù)百種連接分子的Linker庫(kù)。此外,美迪西成熟的計(jì)算機(jī)輔助藥物設(shè)計(jì)技術(shù)平臺(tái),大大提高PROTAC的設(shè)計(jì)合成質(zhì)量。美迪西已經(jīng)驗(yàn)證的PROTAC靶點(diǎn)有:IRAK4, AR, ER, IKZF1, IKZF2, IKZF3, BTK, EGFR, BRD4, BCL-xL, CDK4, CDK6, SMARCA2, SMARCA4, AKT, ALK, STAT3, SHP2, FGFR1, FGFR2, KRAS G12C, KRAS G12D等。
- PROTAC體外研究美迪西案例:HiBiT-標(biāo)簽-POI 穩(wěn)轉(zhuǎn)細(xì)胞株高通量篩選:利用基因敲入技術(shù)構(gòu)建的“內(nèi)源蛋白-HiBiT”穩(wěn)轉(zhuǎn)株細(xì)胞,對(duì)PROTAC分子進(jìn)行高通量篩選,計(jì)算DC50。
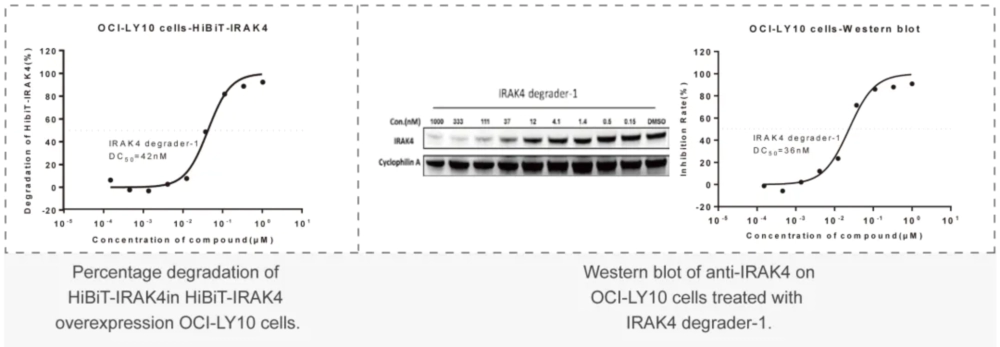 美迪西案例:Western Blot或者In-cell Western:通過(guò)WB實(shí)驗(yàn)檢測(cè)初篩到的PROTAC分子對(duì)靶標(biāo)蛋白的降解能力,分析DC50值。
美迪西案例:Western Blot或者In-cell Western:通過(guò)WB實(shí)驗(yàn)檢測(cè)初篩到的PROTAC分子對(duì)靶標(biāo)蛋白的降解能力,分析DC50值。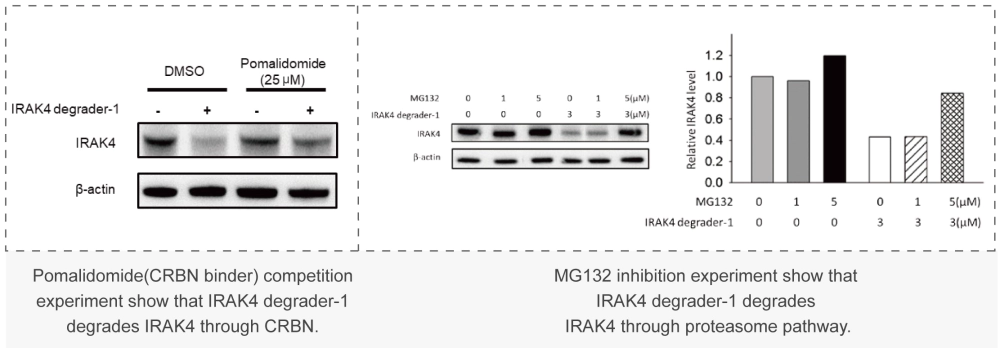 美迪西案例:細(xì)胞毒性實(shí)驗(yàn)(CCK-8或CTG法):檢測(cè)上述篩選到PROTAC對(duì)癌細(xì)胞增殖抑制能力,分析IC50值。
美迪西案例:細(xì)胞毒性實(shí)驗(yàn)(CCK-8或CTG法):檢測(cè)上述篩選到PROTAC對(duì)癌細(xì)胞增殖抑制能力,分析IC50值。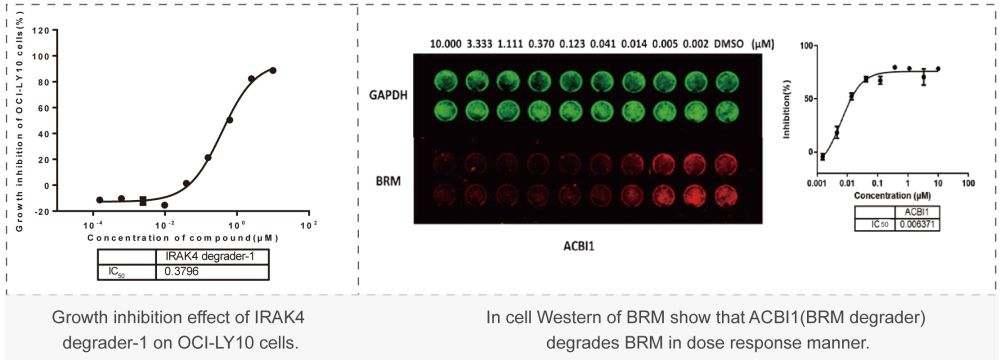
關(guān)于美迪西PPROTAC分子體外評(píng)價(jià)服務(wù)
美迪西建立了完整的PROTAC體外分析平臺(tái),其主要服務(wù)內(nèi)容包括二元及三元復(fù)合物形成分析、靶點(diǎn)泛素化分析以及靶點(diǎn)降解水平分析。這些服務(wù)內(nèi)容涵蓋了從蛋白水平到細(xì)胞水平的多種檢測(cè)方法,能夠?yàn)榭蛻籼峁┤媲腋咝У腜ROTAC分子體外評(píng)價(jià)解決方案。
如果您對(duì)PROTAC體外分析技術(shù)感興趣,請(qǐng)立即聯(lián)系我們,獲取解決方案。
- PROTAC體內(nèi)藥理藥效研究
美迪西藥理藥效部緊跟行業(yè)發(fā)展與市場(chǎng)需求,不斷完善創(chuàng)新,經(jīng)過(guò)多年的經(jīng)驗(yàn)累積,多方驗(yàn)證和長(zhǎng)期實(shí)踐考驗(yàn),建立了完善的動(dòng)物模型庫(kù),可根據(jù)客戶的需求提供各種有效的動(dòng)物模型,用來(lái)檢測(cè)藥物的有效性。實(shí)驗(yàn)動(dòng)物有非人靈長(zhǎng)類動(dòng)物、犬、大小鼠、兔、豚鼠、小型豬等種類。美迪西已建立440+種腫瘤評(píng)價(jià)模型,為多種創(chuàng)新療法賦能。
美迪西案例: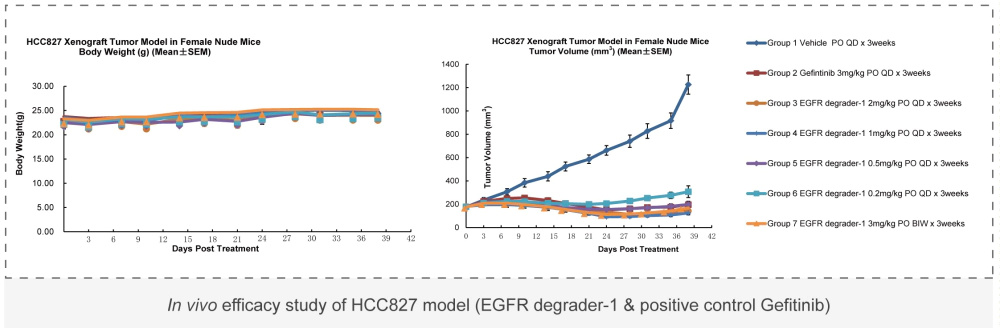
- PROTAC藥代動(dòng)力學(xué)評(píng)價(jià)美迪西DMPK團(tuán)隊(duì),通過(guò)PROTAC技術(shù)原理,結(jié)合研發(fā)案例,利用完善的體外 ADME、體內(nèi)PK測(cè)試平臺(tái),在小分子化合物研究基礎(chǔ)上,建立起一套關(guān)于PROTAC藥物的篩選和IND評(píng)價(jià)體系,關(guān)注藥物的溶解度、滲透性、代謝穩(wěn)定性、代謝產(chǎn)物鑒定與體內(nèi)PK研究等,幫助客戶快速推進(jìn)PROTAC藥物的研發(fā)。美迪西案例:下文中科研人員使用Thalidomide募集Cereblon/cullin 4A E3連接酶并通過(guò) Linker進(jìn)行固化,在小鼠中發(fā)現(xiàn)了具有良好口服藥代動(dòng)力學(xué)特性的高效AR降解劑 ARD-2128。

在此項(xiàng)研究中,科研人員通過(guò)美迪西評(píng)估了五種高效AR降解劑在小鼠中靜脈和口服給藥的藥代動(dòng)力學(xué) (PK) 數(shù)據(jù),其中最優(yōu)化合物為ARD-2128。PK數(shù)據(jù)顯示,ARD-2128具有出色的整體PK曲線:低清除率 (1.2 mL/min/kg) 和中高穩(wěn)態(tài)分布容積 (Vss為2.7 L/kg)。ARD-2128按2 mg/kg劑量靜脈給藥后的T1/2為27.6小時(shí),按5 mg/kg劑量口服給藥后T1/2為18.8小時(shí)。ARD-2128 (5 mg/kg) 在小鼠體內(nèi)達(dá)到67%的口服生物利用度,通過(guò)口服給藥有效降低AR蛋白并抑制腫瘤組織中的AR調(diào)節(jié)基因,從而有效抑制小鼠腫瘤生長(zhǎng)且無(wú)毒性跡象。
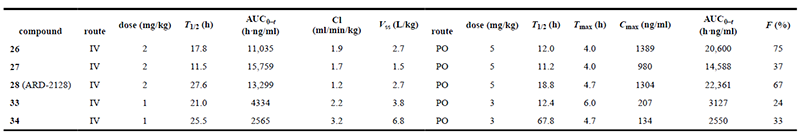 五種化合物在雄性 ICR 小鼠中的 PK 數(shù)據(jù)匯總[1]此外,科研人員通過(guò)美迪西測(cè)試了ARD-2128在小鼠、大鼠、犬、猴和人五種屬中的血漿穩(wěn)定性。數(shù)據(jù)顯示ARD-2128在所有五種屬中都具有穩(wěn)定的血漿穩(wěn)定性。
五種化合物在雄性 ICR 小鼠中的 PK 數(shù)據(jù)匯總[1]此外,科研人員通過(guò)美迪西測(cè)試了ARD-2128在小鼠、大鼠、犬、猴和人五種屬中的血漿穩(wěn)定性。數(shù)據(jù)顯示ARD-2128在所有五種屬中都具有穩(wěn)定的血漿穩(wěn)定性。 ARD-2128 在五種屬中的肝微粒體中代謝穩(wěn)定性和血漿穩(wěn)定性[1]
ARD-2128 在五種屬中的肝微粒體中代謝穩(wěn)定性和血漿穩(wěn)定性[1]
 總結(jié)
總結(jié)- 雖然擁有諸多優(yōu)點(diǎn),但PROTAC藥物開(kāi)發(fā)仍然面臨許多技術(shù)難點(diǎn)。成藥性是其難點(diǎn)。同時(shí),需要尋找更多可用的E3泛素連接酶及其結(jié)合物。此外,還需要考慮如何改善大規(guī)模生產(chǎn)方案,提高產(chǎn)率,從而降低成本。美迪西PROTAC藥物研發(fā)服務(wù)平臺(tái)不僅包含設(shè)計(jì)合成 PROTAC和進(jìn)行PROTAC的體外活性研究,還能對(duì)PROTAC進(jìn)行動(dòng)物體內(nèi)藥效檢測(cè)、藥代動(dòng)力學(xué)研究和安全性評(píng)價(jià)等,并匯總實(shí)驗(yàn)結(jié)果和材料進(jìn)行 IND 申報(bào),以助力客戶加快PROTAC藥物的研發(fā)進(jìn)程。美迪西部分助力PROTAC項(xiàng)目案例——CG001419
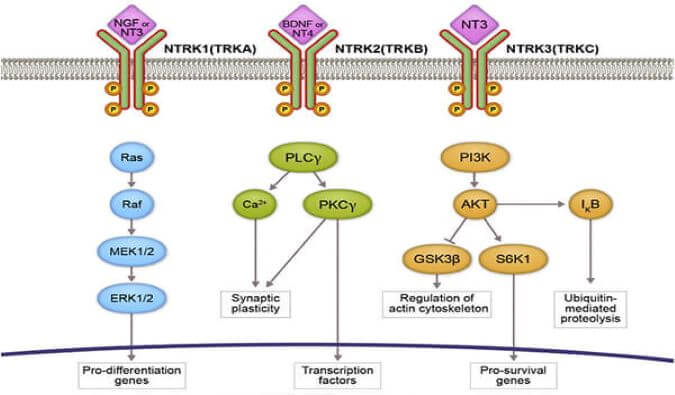
2022年8月,睿躍生物(Cullgen)宣布用于治療晚期實(shí)體瘤的TRK降解劑(CG001419)新藥臨床研究(IND)申請(qǐng)獲批。CG001419是全球首創(chuàng)(First in class)的TRK (神經(jīng)營(yíng)養(yǎng)因子受體酪氨酸激酶)蛋白降解劑。CG001419作為全球首創(chuàng)的高選擇性強(qiáng)效口服靶向蛋白降解劑,其適應(yīng)癥為用于治療治療NTRK基因融合、NTRK基因點(diǎn)突變和NTRK基因擴(kuò)增或過(guò)表達(dá)晚期或轉(zhuǎn)移性成人實(shí)體瘤。作為睿躍生物的合作伙伴,美迪西為CG001419的研發(fā)提供了符合中、美GLP規(guī)范的(包括藥物代謝動(dòng)力學(xué)研究和安全性評(píng)價(jià)在內(nèi)的)綜合性臨床前研究服務(wù),以合規(guī)、高效、高質(zhì)的服務(wù)助力其成功獲批。GT919
2023年5月,標(biāo)新生物分子膠降解劑管線1類新藥GT919膠囊獲得FDA批準(zhǔn)進(jìn)入臨床試驗(yàn),用于惡性血液腫瘤的治療。該管線此前已于2022年12月20日獲得國(guó)家藥品監(jiān)督管理局(NMPA)批準(zhǔn)開(kāi)展臨床試驗(yàn),目前正在中國(guó)進(jìn)行I期臨床研究。
對(duì)于GT919的研發(fā),美迪西憑借扎實(shí)的研發(fā)實(shí)力,高效完成了其從藥物發(fā)現(xiàn)到臨床申報(bào),包括藥物發(fā)現(xiàn)、藥學(xué)研究、臨床前研究等一站式臨床前研究服務(wù)。GT929
2023年10月,標(biāo)新生物第二個(gè)分子膠降解劑管線1類新藥GT929膠囊獲得FDA批準(zhǔn)進(jìn)入臨床試驗(yàn),用于治療惡性血液腫瘤。該管線此前已于2023年7月獲得NMPA批準(zhǔn)開(kāi)展臨床試驗(yàn)。GT929是一款靶向IKZF1/3靶點(diǎn)的分子膠,在彌漫大b細(xì)胞淋巴瘤動(dòng)物模型中顯示了極佳的效果。
作為標(biāo)新生物的戰(zhàn)略合作伙伴,美迪西為GT929的研發(fā)提供了制劑研究、臨床前研究(包括藥效、藥代、安評(píng))以及撰寫中英文申報(bào)資料等服務(wù),為GT929快速實(shí)現(xiàn)中美雙報(bào)雙批提供了技術(shù)保障!獲取更多服務(wù)案例,請(qǐng)聯(lián)系我們:
 推薦閱讀:
推薦閱讀:- 參考文獻(xiàn):[1]. Xin Han, et al. Strategies toward Discovery of Potent and Orally Bioavailable ProteolysisTargeting Chimera Degraders of Androgen Receptor for the Treatment of ProstateCancer. J Med Chem. 2021 Sep9;64(17):12831-12854.
[2]. AyeshaA Shafi, et al. Androgen receptors in hormone-dependent and castration-resistantprostate cancer. PharmacolTher. 2013 Dec;140(3):223-38.
[3]. Weiguo Xiang, et al. Discovery of ARD-2585 as an Exceptionally Potent and Orally Active PROTACDegrader of Androgen Receptor for the Treatment of Advanced Prostate Cancer. J Med Chem. 2021 Sep 23;64(18):13487-13509.
[4]Si-Min Qi, et al. PROTAC: An Effective Targeted Protein Degradation Strategy for Cancer Therapy. Front Pharmacol. 2021 May 7;12:692574.
[5] Galen Andrew Collins, et al. The Logic of the 26S Proteasome. Cell. 2017 May 18;169(5):792-806.
[6]Madhusoodanan Mottamal, et al. From Pure Antagonists to Pure Degraders of the Estrogen Receptor: Evolving Strategies for the Same Target. ACS Omega. 2021 Mar 30;6(14):9334-9343.
[7]Jared A M Bard,et al. Structure and Function of the 26S Proteasome. Annu Rev Biochem. 2018 Jun 20;87:697-724.[8]Xin Lin, et al. Targeting estrogen receptor α for degradation with PROTACs: A promising approach to overcome endocrine resistance. Eur J Med Chem. 2020 Nov 15;206:112689.