



業(yè)務(wù)咨詢
中國(guó):
Email: marketing@medicilon.com.cn
業(yè)務(wù)咨詢專線:400-780-8018
(僅限服務(wù)咨詢,其他事宜請(qǐng)撥打川沙總部電話)
川沙總部電話: +86 (21) 5859-1500
海外:
+1(781)535-1428(U.S.)
0044 7790 816 954 (Europe)
Email:marketing@medicilon.com




2023年3月4日,科鎂信生物聯(lián)合創(chuàng)始人&副總裁張翼博士在基因治療閉門研討會(huì)—美迪西核酸藥物研發(fā)專場(chǎng)中做了主題為《陽(yáng)離子脂質(zhì)高通量定制化篩選》的報(bào)告,本文根據(jù)專家報(bào)告內(nèi)容整理,并經(jīng)專家審核確認(rèn)。

嘉賓簡(jiǎn)介
張 翼 博士
科鎂信生物聯(lián)合創(chuàng)始人&副總裁
2021年回國(guó),聯(lián)合發(fā)起創(chuàng)立科鎂信生物,擔(dān)任副總裁,負(fù)責(zé)公司戰(zhàn)略規(guī)劃,領(lǐng)導(dǎo)開(kāi)發(fā)非病毒基因遞送平臺(tái)。
張博士在Translate Bio(現(xiàn)賽諾菲)、Codiak和Beam therapeutics擁有10年的藥物遞送經(jīng)驗(yàn),專注于核酸療法遞送技術(shù)。在他的整個(gè)職業(yè)生涯中,他致力于開(kāi)發(fā)用于各種核酸治療的LNP輸送平臺(tái)。在Translate Bio和Beam Therapeutics,他是脂質(zhì)發(fā)現(xiàn)團(tuán)隊(duì)的領(lǐng)先科學(xué)家,并發(fā)表了15項(xiàng)關(guān)于新型陽(yáng)離子脂質(zhì)的專利。他在三個(gè)mRNA LNP IND中發(fā)揮了關(guān)鍵作用,并推進(jìn)至臨床。在科迪亞克,他領(lǐng)導(dǎo)了外泌體和核酸純化的工作。
張博士在復(fù)旦大學(xué)獲得高分子科學(xué)理學(xué)士學(xué)位,在德克薩斯大學(xué)達(dá)拉斯西南醫(yī)學(xué)中心獲得生物工程博士學(xué)位,在麻省理工學(xué)院和康奈爾大學(xué)接受了4年的藥物遞送博士后培訓(xùn)。
核酸藥物最大的問(wèn)題就是穩(wěn)定性問(wèn)題,我們知道RNA藥物是一個(gè)中間體,不穩(wěn)定性是其與生俱來(lái)的一個(gè)缺點(diǎn),也是生物進(jìn)化當(dāng)中對(duì)生命健康的一種保護(hù)。那如果要把一個(gè)不穩(wěn)定的RNA這樣一個(gè)中間體做成藥的話,那么一個(gè)有效的保護(hù)體系就是非常重要的。核酸藥物可以大體上分為小核酸和大核酸兩種,第一個(gè)被批準(zhǔn)的siRNA藥物其實(shí)是用LNP來(lái)遞送的,但后來(lái)發(fā)現(xiàn),小核酸是可以通過(guò)化學(xué)合成的,它的主鏈可以通過(guò)化學(xué)修飾而變得更穩(wěn)定。LNP就不是一個(gè)必要的起到保護(hù)作用的遞送載體。但是對(duì)于mRNA或者其他的大核酸來(lái)說(shuō),化學(xué)修飾就不是一個(gè)可行的選擇,因?yàn)閙RNA主鏈不能進(jìn)行任何的修飾,它的不穩(wěn)定性是與生俱來(lái)的。那么LNP對(duì)大核酸來(lái)說(shuō)還是非常重要的一個(gè)遞送載體。
目前LNP臨床階段已驗(yàn)證的應(yīng)用主要有被批準(zhǔn)的Onpattro(siRNA)以及針對(duì)COVID-19的mRNA疫苗,同時(shí)在各管線產(chǎn)品中還有一些拓展應(yīng)用,如CRISPR/Cas基因敲除、基因編輯/基因敲入、RNA編輯、環(huán)狀RNA、體內(nèi)Car-T和腫瘤疫苗。
但是其實(shí)所有潛在的核酸藥物,包括siRNA和mRNA,以及DNA都是LNP可遞送的潛在對(duì)象,只要帶正電,LNP就能對(duì)它進(jìn)行有效包裹和遞送。
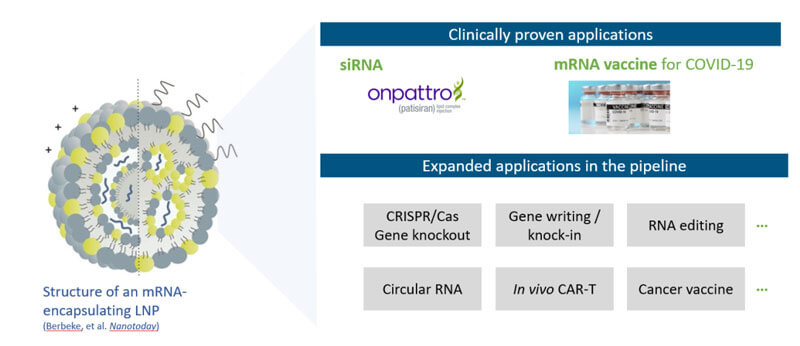
圖1 LNP的結(jié)構(gòu)及其應(yīng)用
我們?nèi)梭w的一些疾病是由于蛋白翻譯不正常造成的,不管是過(guò)高還是過(guò)低,我們都可以通過(guò)這個(gè)RNA藥物來(lái)對(duì)它進(jìn)行治療。所以這個(gè)應(yīng)用場(chǎng)景是非常廣泛的。不同的核酸不同的給藥方式以及不同的靶向性等這些因素是要靠我們的遞送系統(tǒng)來(lái)實(shí)現(xiàn)的。第一步就是要把核酸藥物準(zhǔn)確地、高效地遞送到病灶,從而對(duì)疾病進(jìn)行治療。現(xiàn)在有越來(lái)越多的證據(jù)證明,LNP可以有效地把核酸藥物遞送到不同的組織、不同的器官。
那大家對(duì)現(xiàn)在對(duì)這個(gè)陽(yáng)離子脂質(zhì)的重要性和價(jià)值的認(rèn)識(shí)也越來(lái)越多,有很多工廠和一些新興的公司,都會(huì)采取一個(gè)對(duì)外合作或者收購(gòu)的形式去彌補(bǔ)其在LNP這一塊的缺失。在當(dāng)下LNP研發(fā)環(huán)境中,還是有一些挑戰(zhàn)和機(jī)遇,可以說(shuō)挑戰(zhàn)和機(jī)遇是共存的。其中兩個(gè)是很重要的,第一個(gè)是我們要有自有專利的陽(yáng)離子脂質(zhì),具有全球FTO和獨(dú)占性,就是我們常說(shuō)的被卡脖子的一個(gè)技術(shù)環(huán)節(jié)。第二個(gè)是我們一定要找到適合不同應(yīng)用場(chǎng)景的LNP來(lái)滿足不同的組織靶向性,從不同的給藥途徑來(lái)做出適合不同應(yīng)用條件的基因治療表。
其實(shí)從2000年時(shí),大家就已經(jīng)對(duì)LNP進(jìn)行研發(fā)了,可直到2020年,由于新冠,我們才有了第一個(gè)LNP作為遞送系統(tǒng)的mRNA藥物被批準(zhǔn)。相對(duì)來(lái)說(shuō),這個(gè)發(fā)展還是比較緩慢。那制約LNP發(fā)展的因素主要有以下三方面因素,不同的制約因素也決定了我們采用不同的策略。
我們知道,陽(yáng)離子脂質(zhì)的結(jié)構(gòu)對(duì)于LNP的遞送效率是至關(guān)重要的。大家也在嘗試設(shè)計(jì)不同結(jié)構(gòu)的陽(yáng)離子脂質(zhì),但是到目前為止,大家都沒(méi)能建立一個(gè)有效的構(gòu)效關(guān)系。我們不知道怎樣結(jié)構(gòu)的陽(yáng)離子脂質(zhì)具有高效的遞送效率,具有特殊的靶向性。為解決這個(gè)問(wèn)題,我們采取網(wǎng)篩的策略。也就是說(shuō),如果我們篩100個(gè),篩不到,那我們就篩200個(gè)、500個(gè),甚至1000個(gè),直到篩到我們想要的結(jié)構(gòu)。簡(jiǎn)言之,就是我們篩得越多、越快,就會(huì)有更高的機(jī)率得到一個(gè)我們想要的陽(yáng)離子脂質(zhì)。
我們?cè)诩?xì)胞實(shí)驗(yàn)上,比如篩選出比較好的陽(yáng)離子,就可以把它放到動(dòng)物體內(nèi)去做表征的時(shí)候,發(fā)現(xiàn)這個(gè)藥效完全是一個(gè)相反的結(jié)果。細(xì)胞實(shí)驗(yàn)非常好,然后動(dòng)物實(shí)驗(yàn)當(dāng)中沒(méi)有任何蛋白表達(dá)。也就是說(shuō),在LNP的研發(fā)過(guò)程當(dāng)中,我們沒(méi)有辦法使用傳統(tǒng)的高通量、低成本的細(xì)胞實(shí)驗(yàn)對(duì)其進(jìn)行一個(gè)預(yù)篩選,那我們只能在這個(gè)低通量和高成本的動(dòng)物實(shí)驗(yàn)上對(duì)它進(jìn)行表征。
前面提到LNP的應(yīng)用場(chǎng)景有很多不同的核酸載荷、不同的給藥方式。也就是說(shuō),每一種應(yīng)用場(chǎng)景其實(shí)對(duì)LNP都有一個(gè)特殊的需求。我們發(fā)現(xiàn)不同的核酸、不同的給藥方式,對(duì)不同的LNP有不同偏好。這就使得我們要去對(duì)LNP進(jìn)行一個(gè)定制化的開(kāi)發(fā),讓它適合不同的應(yīng)用場(chǎng)景。
基于這三個(gè)因素,我們覺(jué)得傳統(tǒng)研發(fā)思路不適用于LNP。理想的LNP研發(fā)平臺(tái)需要滿足以下幾點(diǎn):
1. 強(qiáng)大的陽(yáng)離子脂質(zhì)庫(kù);
2. 高通量體內(nèi)篩選;
3. 針對(duì)載荷、靶點(diǎn)以及給藥方式的定制化開(kāi)發(fā)。
其中三大核心能力主要體現(xiàn)在:
我們?cè)O(shè)計(jì)新型脂質(zhì)骨架結(jié)構(gòu),月產(chǎn)出100-1000種高純度陽(yáng)離子脂質(zhì)體來(lái)進(jìn)行內(nèi)部高通量篩選,并且圍繞新型脂質(zhì)體結(jié)構(gòu)申報(bào)具有全球技術(shù)壁壘的知識(shí)產(chǎn)權(quán)。
可應(yīng)用于遞送效率以及不同組織靶向性的動(dòng)物水平的高通量篩選平臺(tái),可以進(jìn)行高效篩選通量可達(dá)每日上百種LNP,且有效節(jié)約成本。
我們針對(duì)不同脂質(zhì)體結(jié)構(gòu)開(kāi)發(fā)最優(yōu)制劑工藝,采用新型生產(chǎn)工藝賦予LNP特殊功能,利用堅(jiān)實(shí)的工藝放大生產(chǎn)產(chǎn)業(yè)經(jīng)驗(yàn)。
這三大核心能力需要解決的事情、實(shí)現(xiàn)的目標(biāo)有兩個(gè):更高遞送效率、更好耐受性的肝靶向陽(yáng)離子脂質(zhì);具有高效肝外靶向的陽(yáng)離子脂質(zhì)。
我們這樣LNP篩選平臺(tái)能夠幫助我們?nèi)ソ鉀Q到一些傳統(tǒng)研發(fā)手段所不能解決的問(wèn)題。這個(gè)篩選的起點(diǎn)都是從我們具有自主知識(shí)產(chǎn)權(quán)的陽(yáng)離子脂質(zhì)庫(kù)開(kāi)始的。我們會(huì)對(duì)所有合成出來(lái)的陽(yáng)離子脂質(zhì),通過(guò)靜脈給藥的方式,進(jìn)行一個(gè)體內(nèi)藥效的初篩,得到高藥效脂質(zhì)。然后我們?cè)贂?huì)把這部分篩選出來(lái)陽(yáng)離子脂質(zhì),在動(dòng)物實(shí)驗(yàn)上進(jìn)行進(jìn)一步的篩選。比如,除了靜脈給藥方式,我們也會(huì)考察其他的給藥方式,看不同LNP適合哪種給藥方式,我們同樣也會(huì)從核酸載荷和靶向性方面進(jìn)行定制化篩選。然后我們還將這些LNP進(jìn)行進(jìn)一步的耐受性篩選。最終篩選到的少數(shù)LNP被認(rèn)為是藥效高、耐受性好的LNP。(如圖2)
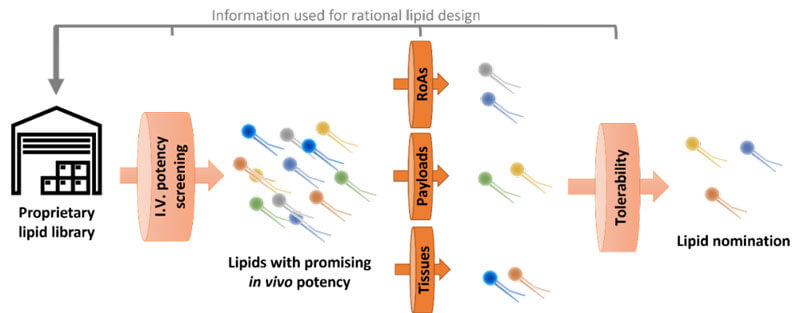
圖2 科鎂信LNP篩選流程
通過(guò)設(shè)計(jì)并篩選“成千上萬(wàn)”個(gè)陽(yáng)離子脂質(zhì),我們能:
1.根據(jù)不同應(yīng)用定制LNP;
2.拓寬新的專利空間;
3.加快建立基于大數(shù)據(jù)分析得到的構(gòu)效關(guān)系,從而指導(dǎo)陽(yáng)離子脂質(zhì)結(jié)構(gòu)設(shè)計(jì)。
接下來(lái),張翼博士還分享了科鎂信LNP高通量篩選平臺(tái)取得的一些進(jìn)展。首先是高通量合成和篩選方面,在過(guò)去的半年多時(shí)間內(nèi),我們已經(jīng)合成并篩選了700個(gè)自主知識(shí)產(chǎn)權(quán)的陽(yáng)離子脂質(zhì),并希望在今年年底,這個(gè)數(shù)量能夠達(dá)到2500個(gè),篩的更多,篩的更快,從而得到更好的陽(yáng)離子脂質(zhì)結(jié)構(gòu)。
同時(shí)我們也評(píng)估了這些我們?cè)O(shè)計(jì)出來(lái)的陽(yáng)離子脂質(zhì)的體內(nèi)核酸遞送效率,找到了有80個(gè)陽(yáng)離子脂質(zhì),表現(xiàn)出了比MC3 LNP更高的蛋白表達(dá)效率,其中有兩個(gè)LNP是達(dá)到十倍的翻譯效率。那我會(huì)把這80個(gè)LNP放到其他的應(yīng)用場(chǎng)景上,進(jìn)行進(jìn)一步的篩選。那我們針對(duì)這80個(gè)LNP當(dāng)中挑選出適合不同應(yīng)用場(chǎng)景的LNP,即進(jìn)行定制化篩選。比如適合靜脈給藥的CPL-180和CPL-092, 適合肌肉給藥的CPL-457, 適合基因編輯工具的CPL-455,以及適合靶向T細(xì)胞的CPL-180等。
除了陽(yáng)離子脂質(zhì)篩選呢,我們也會(huì)利用我們獨(dú)特的工藝開(kāi)發(fā)優(yōu)勢(shì)解決LNP目前的一些短板。
1. 第一個(gè)優(yōu)勢(shì)就是解決耐受性問(wèn)題。我們知道陽(yáng)離子脂質(zhì)是作為一個(gè)帶正電的小分子,它的生物安全性、耐受性始終是被大家詬病了一個(gè)地方。大家采取一個(gè)策略就是不斷的降低它的劑量來(lái)去減緩這個(gè)問(wèn)題。但降低劑量的同時(shí),又將出現(xiàn)一個(gè)藥效問(wèn)題。而我們就可以用相同的LNP去做到更高的蛋白表達(dá)。從數(shù)據(jù)看,科鎂信獨(dú)有的生產(chǎn)工藝可提高M(jìn)C3 LNP和ALC-0315 LNP的體內(nèi)藥效,在藥效和耐受性之間取得一個(gè)平衡。
2. 第二個(gè)優(yōu)勢(shì)就是我們通過(guò)自主工藝的開(kāi)發(fā),做出了穩(wěn)定的LNP,同時(shí)我們發(fā)現(xiàn)在老鼠體上還具有更高的蛋白表達(dá)效率。數(shù)據(jù)證明,得到的穩(wěn)定PEG-free ALC-0315 LNP有更高的體內(nèi)藥效。因?yàn)槲覀冎繪NP和mRNA藥物通常是需要重復(fù)給藥的,那人體內(nèi)的anti-PEG抗體會(huì)識(shí)別并清除所有LNP。在我們以往的研發(fā)過(guò)程中,發(fā)現(xiàn)LNP給藥次數(shù)越多,藥效就會(huì)降低。那如果我們做出一個(gè)穩(wěn)定的PEG-free的LNP,就能從根源上去解決這個(gè)問(wèn)題。
3. 第三個(gè)優(yōu)勢(shì)是我們通過(guò)工藝開(kāi)發(fā)方式,通過(guò)增加LNP表面修飾,達(dá)到主動(dòng)靶向性。到目前為止,LNP都是被動(dòng)的靶向。解決這個(gè)問(wèn)題辦法就是增加LNP表面的修飾。主要一個(gè)難點(diǎn)就是怎么將靶頭接到LNP的表面。因?yàn)槲覀冎繪NP是利用正電和負(fù)電的相互吸引,來(lái)形成一個(gè)自組裝的結(jié)構(gòu)。如果我們把一個(gè)富集電荷的結(jié)構(gòu)(如多肽),接到LNP表面上的話,會(huì)極大地影響LNP的穩(wěn)定性,不能夠穩(wěn)定存在,就不能工藝放大。
然后另外一點(diǎn)是,我們知道很多這種帶有主動(dòng)靶向性的靶頭、帶有功能性的靶頭,通常都是帶正電的。在我們傳統(tǒng)的工藝下,這些帶正電的靶頭會(huì)傾向于和帶負(fù)電荷的核酸結(jié)合成complex,而不是按照我們?cè)O(shè)計(jì)主動(dòng)的去待在LNP的表面。所以說(shuō)這個(gè)LNP的表面修飾是比較難做到的一個(gè)事情。那目前我們也是通過(guò)一些工藝的優(yōu)化,做出多肽修飾的LNP。我們發(fā)現(xiàn)沒(méi)有修飾的LNP,它在脾臟上面是沒(méi)有任何的表達(dá)。然后我們修飾之后,我們可以看到脾臟的蛋白表達(dá)有極大的提高。實(shí)驗(yàn)表明,表面修飾的LNP表現(xiàn)出主動(dòng)靶向性。
最后張翼博士總結(jié)了科鎂信陽(yáng)離子脂質(zhì)高通量篩選平臺(tái)的三個(gè)驅(qū)動(dòng)引擎:
每月能生產(chǎn)~1g mRNA以支持體內(nèi)篩選實(shí)驗(yàn)。工藝開(kāi)發(fā)至百克級(jí)別 mRNA生產(chǎn),以支持管線開(kāi)發(fā)。單通道混合生產(chǎn)達(dá)20g LNP。
每周300只小鼠協(xié)助體內(nèi)篩選。并且具有超10種不同給藥方式進(jìn)行定制化篩選。
每月測(cè)試1-2個(gè)新的脂質(zhì)家族 ;每月合成200個(gè)高純度科鎂信專利結(jié)構(gòu)脂質(zhì);每月合成~1000個(gè)LNP。我們相信在這三個(gè)引擎的推動(dòng)下,科鎂信今后能更好地去迭代陽(yáng)離子脂質(zhì),然后找出適合我們臨床應(yīng)用的陽(yáng)離子脂質(zhì)。
LNP是核酸類藥物的核心和價(jià)值所在。但陽(yáng)離子脂質(zhì)結(jié)構(gòu)設(shè)計(jì)鮮有指導(dǎo)原則、體內(nèi)篩選實(shí)驗(yàn)低通量和高成本、以及缺乏針對(duì)不同核酸載荷/給藥方式的定制化開(kāi)發(fā)這個(gè)三方面制約了LNP的發(fā)展。基于制約因素,科鎂信LNP團(tuán)隊(duì)設(shè)計(jì)新型脂質(zhì)骨架結(jié)構(gòu),建立高通量LNP篩選平臺(tái),開(kāi)發(fā)最優(yōu)制劑工藝,實(shí)現(xiàn)獲得更高遞送效率、更好耐受性的肝靶向LNP,以及具有高效肝外靶向的LNP的目標(biāo)。
