



業(yè)務(wù)咨詢
中國(guó):
Email: marketing@medicilon.com.cn
業(yè)務(wù)咨詢專(zhuān)線:400-780-8018
(僅限服務(wù)咨詢,其他事宜請(qǐng)撥打川沙總部電話)
川沙總部電話: +86 (21) 5859-1500
海外:
+1(781)535-1428(U.S.)
0044 7790 816 954 (Europe)
Email:marketing@medicilon.com





當(dāng)一種原料藥完全或部分以固體狀態(tài)存在于藥品中時(shí),其物理狀態(tài)(晶習(xí)、晶型、顆粒大小、粒徑分布)在開(kāi)發(fā)、制劑以及產(chǎn)品整個(gè)生命周期內(nèi)發(fā)生變化是不能接受的。這適用于所有固體制劑、半固體制劑、混懸劑以及固體分散體。
藥物的固態(tài)形式不同可能具有不同的物理和化學(xué)性質(zhì),例如:堆積性質(zhì)(密度、吸濕性等)、熱力學(xué)性質(zhì)(溶解度、熵焓、自由能等)、光學(xué)性質(zhì)、動(dòng)力學(xué)性質(zhì)(溶解速率、穩(wěn)定性等)、表面性質(zhì)(晶習(xí)、表面自由能等)、機(jī)械性質(zhì)(流動(dòng)性、壓縮性等)。可能對(duì)原料藥及制劑的穩(wěn)定性、制劑的生產(chǎn)工藝、溶出度及生物利用度等產(chǎn)生影響,進(jìn)而可能影響藥物的安全性、有效性和質(zhì)量可控性。
監(jiān)管機(jī)構(gòu)要求對(duì)藥物的多態(tài)性進(jìn)行徹底的篩選,要求藥企對(duì)其中一種形式或規(guī)定的混合形式做出經(jīng)證實(shí)的選擇。美國(guó)藥監(jiān)局(FDA)和中國(guó)藥監(jiān)局(NMPA)在藥物申報(bào)中對(duì)此提出了明確規(guī)定,要求對(duì)藥物多晶型現(xiàn)象進(jìn)行研究并提供相應(yīng)數(shù)據(jù)。藥物固態(tài)研究可作為提高藥物成藥性、降低開(kāi)發(fā)風(fēng)險(xiǎn)、保證產(chǎn)品質(zhì)量和建立有效專(zhuān)利壁壘等的重要手段,固態(tài)形式是連接藥物分子與藥品的橋梁。因此,開(kāi)發(fā)“正確”的固體形式對(duì)于產(chǎn)品的成功至關(guān)重要。
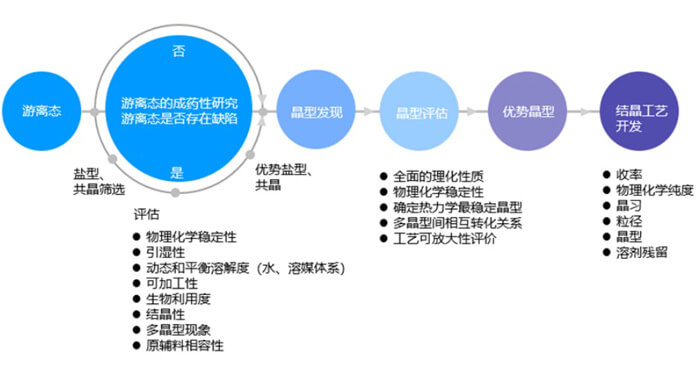
首先,當(dāng)臨床前候選化合物PCC確定之后,需要考慮的第一個(gè)問(wèn)題是開(kāi)發(fā)鹽、共晶還是游離態(tài)?在創(chuàng)新藥的研發(fā)過(guò)程中,早期非臨床評(píng)價(jià)期間,以達(dá)到動(dòng)物給藥的暴露量為目的,若游離態(tài)形式已經(jīng)可以滿足要求且物理化學(xué)性質(zhì)穩(wěn)定,則沒(méi)有必要開(kāi)發(fā)鹽型。基于開(kāi)發(fā)的角度,API越“簡(jiǎn)單”對(duì)于制劑的一系列工藝開(kāi)發(fā)放大及生產(chǎn)越有好處。游離態(tài)直接進(jìn)行晶型研究的前提是需要對(duì)該自由堿有全面清晰的認(rèn)知,進(jìn)行系統(tǒng)全面的理化性質(zhì)表征,識(shí)別出化合物的特點(diǎn),以判斷該其是否適合進(jìn)行后續(xù)的制劑開(kāi)發(fā)。
若游離態(tài)穩(wěn)定且生物利用度高,那么直接進(jìn)行晶型研究即可。因?yàn)槌甥}或共晶通常需要在合成中增加一個(gè)額外的生產(chǎn)工藝步驟,而且由于鹽或共晶體的分子量總是高于游離態(tài)分子,對(duì)離子使有效活性成分含量降低,另外還有就是對(duì)離子的潛在毒性等,因此只有當(dāng)鹽或共晶與游離酸/堿相比具有明顯的優(yōu)勢(shì)時(shí),才會(huì)選擇它們。通常,如果游離酸/堿至少具有以下不良性質(zhì)之一,則選擇鹽或共晶:
?溶解度低
?結(jié)晶度低或者無(wú)法結(jié)晶
?熔點(diǎn)低
?高吸濕性
?生物利用度不好
?化學(xué)不穩(wěn)定
?非理想的固體形式,如隧道水合物或存在互變多晶型(轉(zhuǎn)變溫度接近室溫),無(wú)水物和水合物互變(轉(zhuǎn)變濕度在日常濕度范圍)
?知識(shí)產(chǎn)權(quán)問(wèn)題
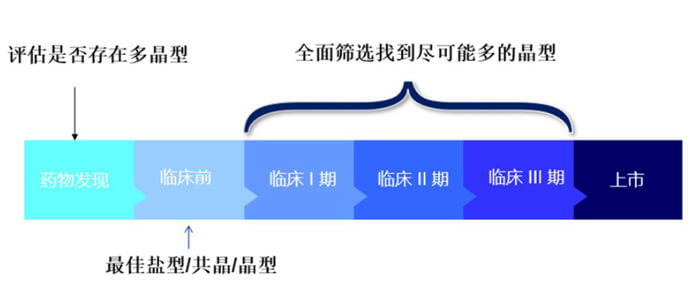
不同的開(kāi)發(fā)階段可以進(jìn)行不同的篩選工作,建議在臨床前的藥學(xué)研究(對(duì)照品、標(biāo)樣的合成與標(biāo)化前)確定鹽型和熱力學(xué)穩(wěn)定晶型。在藥物進(jìn)行IND申報(bào)前確定鹽型,因?yàn)椴煌柠}型屬于不同新化學(xué)實(shí)體(NCE),在研究后期進(jìn)行鹽型轉(zhuǎn)變,可能要面對(duì)雜質(zhì)譜的變化、制劑處方的重新開(kāi)發(fā)和穩(wěn)定性的重新考察,甚至臨床方面的橋接,如毒理橋接,生物等效性橋接等。晶型的篩選及最終確定則是緊跟著鹽型篩選工作,但需要注意的是NCE從研發(fā)到上市可能需要經(jīng)過(guò)多輪的晶型篩選。
臨床前階段的晶型篩選是為了快速確定后續(xù)制劑開(kāi)發(fā)所用的晶型,使用該晶型加速臨床樣品研發(fā)及生產(chǎn)。隨著產(chǎn)品工藝開(kāi)發(fā)的深入,還有可能需要在臨床I期或是臨床II期階段,需要進(jìn)行更廣泛的篩選。首先是出于專(zhuān)利申請(qǐng)的考慮;更重要的是利用這段空檔時(shí)間查看有無(wú)更穩(wěn)定的晶型。
由于臨床前階段API的量和純度,限制了無(wú)法在該階段完成廣泛的晶型篩選,且多晶型的出現(xiàn)受化合物純度影響,若基于臨床I期/II期的具有代表性且化合物純度更高的批次,對(duì)起始物進(jìn)行篩選,則可能會(huì)找到更穩(wěn)定的晶型。雜質(zhì)可以通過(guò)影響成核和生長(zhǎng)速率來(lái)影響它們?cè)谌芤汉蛻腋∫褐械膭?dòng)力學(xué)穩(wěn)定性。因此,用早期批次的仍含有許多雜質(zhì)的原料藥進(jìn)行的多晶型篩選可能與用較晚、較純的批次進(jìn)行的篩選獲得不同的結(jié)果。在特別糟糕的情況下,在初步篩選中可能沒(méi)有發(fā)現(xiàn)優(yōu)勢(shì)的固態(tài)形式。因此,建議用最終GMP生產(chǎn)的一批具有待上市產(chǎn)品的雜質(zhì)特征原料藥,至少重復(fù)有限的多晶型篩選。
以什么樣品的固態(tài)形式進(jìn)行開(kāi)發(fā)(熱力學(xué)穩(wěn)定晶型或亞穩(wěn)晶型):通常是選擇熱力學(xué)穩(wěn)定晶型開(kāi)發(fā),因?yàn)樵跊](méi)有溶劑和濕度的情況下,室溫下熱力學(xué)穩(wěn)定的晶型是唯一保證不會(huì)轉(zhuǎn)晶的晶型。當(dāng)然這不是絕對(duì)的情況,比如以下原因,可能會(huì)選擇亞穩(wěn)晶型開(kāi)發(fā)。
?穩(wěn)定晶型的溶解度和生物利用度太低
?所需高溶解速率的速釋劑
?不同的多晶型物具有不同的機(jī)械性能,例如硬度、粉末流動(dòng)性、可壓縮性和粘合強(qiáng)度。一個(gè)著名的例子是對(duì)乙酰氨基酚,其中熱力學(xué)穩(wěn)定形式(單斜晶型 I)不能壓制成穩(wěn)定的片劑,而亞穩(wěn)型 II(正交晶型)可以,因?yàn)樗谒苄宰冃畏矫姹憩F(xiàn)出更有利的特性。
?穩(wěn)定晶型制造困難
?IP問(wèn)題
?由于拓?fù)浠瘜W(xué)因素,熱力學(xué)穩(wěn)定晶型的化學(xué)不穩(wěn)定性定
藥物固態(tài)開(kāi)發(fā),開(kāi)發(fā)到什么程度,開(kāi)發(fā)的質(zhì)量如何評(píng)估,通常只需要問(wèn)自己以下幾個(gè)問(wèn)題:那種晶型應(yīng)該用于開(kāi)發(fā),這種晶型是否能夠可靠的生產(chǎn)出來(lái),如何確保在配方和產(chǎn)品的保質(zhì)期內(nèi)不發(fā)生不希望發(fā)生的變化?如果以上問(wèn)題都能很好的答復(fù),那么,恭喜你,你開(kāi)發(fā)的固體形態(tài)基本沒(méi)問(wèn)題。
?藥物開(kāi)發(fā)必須全面篩選和充分評(píng)估藥物的多晶型現(xiàn)象,確定優(yōu)勢(shì)鹽型和優(yōu)勢(shì)晶型,以助藥品在臨床上實(shí)現(xiàn)最佳表現(xiàn)。
?在新藥開(kāi)發(fā)的過(guò)程中,藥化階段確定PCC之后,快速拿到足夠用于固態(tài)研究樣品,盡快確定開(kāi)發(fā)的優(yōu)勢(shì)鹽型和優(yōu)勢(shì)晶型有利于推進(jìn)藥物IND階段的研發(fā)進(jìn)度,加速I(mǎi)ND申報(bào)。
?如何廣泛地開(kāi)展固體形態(tài)的篩選是一個(gè)困難的決定。非常廣泛的篩選會(huì)獲得更好、更安全的產(chǎn)品和廣泛的專(zhuān)利保護(hù),同時(shí)增加開(kāi)發(fā)成本。篩選的方案設(shè)計(jì)至關(guān)重要,以最少的實(shí)驗(yàn)工作,探索出盡可能多的形式。
?無(wú)論進(jìn)行多么徹底的篩選,仍然存在一個(gè)不可避免的問(wèn)題:是否真的找到了最穩(wěn)定的形式?沒(méi)有科研人員或?qū)<覍W(xué)者能夠給出100%確信的答案,因?yàn)閬喎€(wěn)態(tài)晶型可能在相對(duì)較長(zhǎng)的時(shí)間內(nèi)保持其動(dòng)力學(xué)穩(wěn)定性。
?從統(tǒng)計(jì)學(xué)的角度來(lái)說(shuō),鹽型/晶型不發(fā)生改變,幾乎不存在,更不符合熱力學(xué)規(guī)律藥物固態(tài)研發(fā)團(tuán)隊(duì)工作的核心在于:盡可能減少鹽型/晶型在后期開(kāi)發(fā)中發(fā)生改變的風(fēng)險(xiǎn)。
[1] Drugs and the pharmaceutical sciences, Vol. 192
[2] Polymorphism in the Pharmaceutical Industry: Solid Form and Drug Development
[3] Pharmaceutical Salts and Co-crystals
[4] Crystallization of Organic Compounds
美研|CMC系列回顧
? CMC系列(一):淺談藥物研發(fā)中原料藥工藝研究的重要性