



業務咨詢
中國:
Email: marketing@medicilon.com.cn
業務咨詢專線:400-780-8018
(僅限服務咨詢,其他事宜請撥打川沙總部電話)
川沙總部電話: +86 (21) 5859-1500
海外:
+1(781)535-1428(U.S.)
0044 7790 816 954 (Europe)
Email:marketing@medicilon.com




通常來說,生物等效性(BE)試驗是指用生物利用度研究的方法,以藥代動力學參數為指標,比較同一種藥物的相同或者不同劑型的制劑,在相同的試驗條件下,其活性成分吸收程度和速度有無統計學差異的人體試驗。對于仿制藥來說,生物等效性(BE)試驗是一個判定仿制藥與參比制劑或對照藥物最終是否一致的“金標準”。
但是對于一些藥物,例如磷結合劑或膽汁酸結合劑等制劑來說,該類藥物因無法吸收入血,僅在胃腸道局部產生作用,無法通過測定血藥濃度的方法,來比較不同制劑間的差異推測其臨床治療效果的差異性,對于該類型制劑,參考FDA、EMA和NMPA等相關指導原則或指南,可采用體外研究如結合平衡試驗和結合動力學試驗作為有效性評價的方法,以代替傳統的藥代動力學為終點的人體生物等效性研究。
美迪西制劑部門胃腸道藥物體外生物等效性(BE)研究服務平臺是在依托良好的質量體系、多樣的質量分析研究設備和豐富的藥物研究及申報經驗基礎上,建立的主要針對在胃腸道產生局部作用且無法進行體內等效性評價的藥物開展相關試驗的研究平臺,致力于為客戶提供仿制藥開發中的體外生物等效性研究服務,并有該類藥物的研究評價和申報經驗。
◆ 適用于體外生物等效性評價研究的藥物
◆ 體外磷結合平衡研究試驗及動力學試驗
◆ 體外膽汁酸鹽結合平衡試驗及動力學試驗
◆ 體外HSA或BSA蛋白結合試驗
◆ 體外胃蛋白酶結合試驗(酶活性抑制研究)
◆ 體外BE方法開發及驗證
◆ 體外BE統計分析及判定
◆ 其他需要采取體外酶結合或蛋白結合試驗預估新藥或新化合物在胃腸道作用的研究
? 檢測方法開發
? HPLC or UV or IC or MS
? 方法學驗證
? 專屬性
? 靈敏度
? 定量限
? 線性
? 重復性
? 中間精密度
? 準確度
? 耐用性(檢測方法及儀器參數)

? 樣品狀態及預處理
? 被吸附物濃度范圍最大濃度
? 孵育時間
? 其他參數
? 標難溶液曲線
? 重復至少12組
? 空白試驗

? 樣品狀態及預處理
? 被吸附物濃度2~3個
? 孵育時間
? pH值監測及穩態時間
? 標難溶液曲線
? 結合百分比和結合量
? 空白試驗
? 重復至少12組
? 快速上升段及平合特征
? 結合比率

? Langmuir方程計算k1、k2
? 90%置信區間
? 自由度
? T檢驗或f2相似法
? 其他

? 研究例數與統計
? 異常原因調查
? 最終處理與判定
對于在胃腸道產生局部作用且無法進行體內等效性評價的藥物,美迪西也擁有相關項目品種的體外生物等效性評價經驗,如碳酸司維拉姆片、硫糖鋁口服混懸液等,且部分相關項目已推進至CDE評審階段。
美迪西重視研究項目質量的合規性、真實性和完整性,嚴格按照FDA、NMPA相關法規和指南開展研究試驗,有多次接受并通過國家藥品審評中心項目現場核查的經驗。截止目前,參與研發完成的新藥及仿制藥項目已有超過385件獲得批件。
美迪西制劑部門分析團隊擁有豐富的新藥與仿制藥方法開發、驗證及申報經驗,熟悉國內外注冊法規對于體外生物等效性研究的法規要求,部門負責人深耕藥物研究幾十年,在制劑研究及藥品注冊方面經驗豐富,項目負責人擁有相關體外生物等效性研究的項目經驗,且有多個主要負責的新藥項目和仿制藥研究項目獲得批件。
美迪西成立近20年以來,致力于為全球企業、研究機構及科研工作者提供全方位的臨床前新藥研究服務(包括原料及制劑藥學研究、藥代動力學和安全性評價研究、IND注冊申報等)和仿制藥藥學研究服務(包括仿制藥逆向解析,處方工藝研究、質量控制研究及穩定性研究、體外生物等效性評價等)。配備各類優質且齊全的質量分析研究設備(如多品牌HPLC和溶出儀、UPLC、LC-MS、IC、GC、生物分析儀、疊加式恒溫培養振蕩器(可容納40個500ml固定架)等),以匹配不同研究劑型或分析檢測目所需,研究項目涉及固體、液體、注射劑、半固體、吸入制劑、脂質體等不同類型的制劑,助力客戶項目順利獲批,加速新藥研發進程和仿制藥的上市。


| 品名 | 作用機制 | 服用方法 | FDA指南體外BE評價方式 | 內容 |
| 碳酸司維拉姆片 | 不會被人體吸收的交聯聚合物, 口服進入胃部后,在胃酸的作用下,生成鹽酸司維拉姆,這些胺基會在腸道內以離子交換與磷酸分子結合,形成不溶于水的磷酸司維拉姆復合物,最終通過食物殘渣和糞便排出體外。 | 隨餐服用 | API的一致性 | 包括固態NMR(13C-1H偏振)、IR、拉曼、DSC、XRD、EA、碳酸鹽含量、總可滴定胺、溶脹指數和粒度分布等 |
| 磷酸鹽結合平衡試驗 | 處理:無酸處理的pH4和pH7 | |||
| 處理:經酸處理的pH4和pH7 | ||||
| 磷酸鹽結合動力學試驗 | 處理:無酸處理的pH4和pH7 濃度:最低濃度和最高濃度 | |||
| 處理:經酸處理的pH4和pH7 濃度:最低濃度和最高濃度 |
關鍵參數:
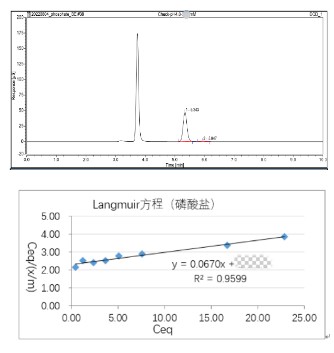
※ 酸濃度及體積
※ 酸預處理時間
※ 不同濃度磷酸鹽設置
※ pH值監測與穩態時間
※ 孵化時間
| 品名 | 作用機制 | 服用方法 | FDA指南體外BE評價方式 |
| 硫糖鋁口服混懸液 | 胃黏膜保護劑,用于慢性胃炎及緩解胃酸過多引起的胃痛、胃灼熱感(燒心)、反酸。在酸性環境中與胃內滲出蛋白質結合成凝膠狀覆蓋于胃黏膜表面,阻止 H 彌散。結合胃蛋白酶使其失活 | 餐前1小時及睡前服用 | API的一致性研究 |
| 膽汁酸鹽結合平衡試驗 | |||
| 膽汁酸鹽結合動力學試驗 | |||
| BSA結合試驗 | |||
| 胃蛋白酶結合試驗 |
關鍵參數(膽汁酸鹽結合):
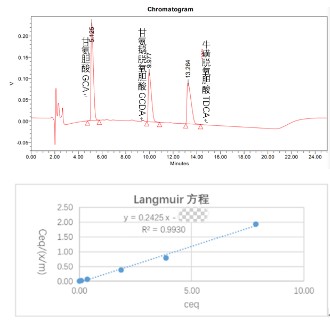
※ 酸濃度及體積
※ 酸預處理時間
※ 膽汁酸鹽組成及濃度設置
※ pH值
※ 穩態時間
※ 孵化時間
關鍵參數(胃蛋白酶結合):
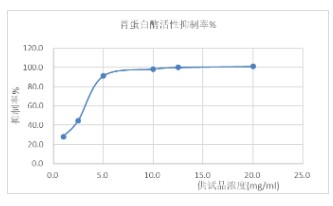
※ 胃蛋白酶濃度
※ 反應過程控制
※ 酸濃度及體積
※ 酸預處理時間
※ 檢測方法
 相關新聞
相關新聞